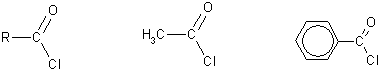
Нитриловые перчатки. Откуда взялся нитрил, что это такое и как правильно его использовать? Нитрилы карбоновых кислот Каталитическое окисление бутана
Способы получения . 1 . Окисление альдегидов и первичных спиртов - общий способ получения карбоновых кислот. В качестве окислителей применяются />K М n О 4 и K 2 С r 2 О 7 .
2 Другой общий способ - гидролиз галогензамещенных углеводородов, содержащих, три атома галогена у одного атома углерода. При этом образуются спирты, содержащие группы ОН у одного атома углерода - такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:/>
| ЗNаОН | ||||
| R-CCl 3 | → | R — COOH + Н 2 О | ||
| -3NaCl |
3 . Получение карбоновых кислот из цианидов (нитрилов) - это важный способ, позволяющий наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия, например:/>
СН 3 -В r + NaCN → CH 3 — CN + NaBr .
Образующийся нитрил уксусной кислоты (метилцианид) при нагревании легко гидролизуется с образованием ацетата аммония:
CH 3 CN + 2Н 2 О → CH 3 COONH 4 .
При подкислении раствора выделяется кислота:
CH 3 COONH 4 + HCl → СН 3 СООН + NH 4 Cl .
4 . Использование реактива Гриньяра по схеме:/>
Н 2 О
R
—
MgBr
+ СО 2 →
R
—
COO
—
MgBr
→
R
—
COOH
+
Mg
(OH
)
Br
5 . Гидролиз сложных эфиров:/>
R — COOR 1 + КОН → R — COOK + R ‘ OH ,
R — COOK + HCl → R — COOH + KCl .
6 . Гидролиз ангидридов кислот:/>
(RCO ) 2 O + Н 2 О → 2 RCOOH .
7 . Для отдельных кислот существуют специфические способы получения./>
Муравьиную кислоту получают нагреванием оксида углерода ( II ) с порошкообразным гидроксидом натрия под давлением и обработкой полученного формиата натрия сильной кислотой:
Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха:
2С 4 Н 10 + 5 O 2 → 4СН 3 СООН + 2Н 2 О.
Для получения бензойной кислоты можно использовать окисление монозамешенных гомологов бензола кислым раствором перманганата калия:
5С 6 Н 5 -СН 3 + 6 KMnO 4 + 9 H 2 SO 4 = 5С 6 Н 5 СООН + 3 K 2 SO 4 + 6 MnSO 4 + 14 H 2 O .
Кроме того, бензойную кислоту можно получить из бензальдегида с помощью реакции Канниццаро . В этой реакции бензальдегид обрабатывают 40-60%-ным раствором гидроксида натрия при комнатной температуре. Одновременное окисление и восстановление приводит к образованию бензойной кислоты и соответственно фенилметанола (бензилового спирта):
Химические свойства . Карбоновые кислоты - более сильные кислоты, чем спирты, поскольку атом водорода в карбоксильной группе обладает повышенной подвижностью благодаря влиянию группы СО. В водном растворе карбоновые кислоты диссоциируют:/>
RCOOH
![]() RCOO — + Н +
RCOO — + Н +
Тем не менее из-за ковалентного характера молекул карбоновых кислот указанное выше равновесие диссоциации достаточно сильно сдвинуто влево. Таким образом, карбоновые кислоты - это, как правило, слабые кислоты. Например, этановая (уксусная) кислота характеризуется константой диссоциации К а = 1,7*10 -5 . />
Заместители, присутствующие в молекуле карбоновой кислоты, сильно влияют на ее кислотность вследствие оказываемого ими индуктивного эффекта . Такие заместители, как хлор или фенильный радикал оттягивают на себя электронную плотность и, следовательно, вызывают отрицательный индуктивный эффект (-/). Оттягивание электронной плотности от карбоксильного атома водорода приводит к повышению кислотности карбоновой кислоты. В отличие от этого такие заместители, как алкильные группы, обладают электронодонорными свойствами и создают положительный индуктивный эффект, +I. Они понижают кислотность. Влияние заместителей на кислотность карбоновых кислот наглядно проявляется в значениях констант диссоциации K a для ряда кислот. Кроме того, на силу кислоты оказывает влияние наличие сопряженной кратной связи.
|
Карбоновые кислоты Формула K a |
|
Пропионовая CH 3 CH 2 COOH 1,3*10 -5 |
|
Масляная CH 3 CH 2 CH 2 COOH 1,5*10 -5 |
|
Уксусная CH 3 COOH 1,7*10 -5 |
|
Кротоновая CH 3 — CH = CH — COOH 2,0*10 -5 |
|
Винилуксусная CH 2 =CH-CH 2 COOH 3,8*10 -5 |
|
Акриловая CH 2 =CH-COOH 5,6*10 -5 |
|
Муравьиная HCOOH 6,1*10 -4 |
|
Бензойная C 6 H 5 COOH 1,4*10 -4 |
|
Хлоруксусная CH 2 ClCOOH 2,2*10 -3 |
|
Тетроновая CH 3 — C ≡ C — COOH 1,3*10 -3 |
|
Дихлоруксусная CHCl 2 COOH 5,6*10 -2 |
|
Щавелевая HOOC — COOH 5,9*10 -2 |
|
Трихлоруксусная CCl 3 COOH 2,2*10 -1 |
Взаимное влияние атомов в молекулах дикарбоновых кислот приводит к тому, что они являются более сильными, чем одноосновные.
2. Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот. Они реагируют с активными металлами, основными оксидами, основаниями и солями слабых кислот:
2 RCOOH + М g → (RCOO ) 2 Mg + Н 2 ,
2 RCOOH + СаО → (RCOO ) 2 Ca + Н 2 О,
RCOOH + NaOH → RCOONa + Н 2 О,
RCOOH + NaHCO 3 → RCOONa + Н 2 О + СО 2 .
Карбоновые кислоты - слабые, поэтому сильные минеральные кислоты вытесняют их из соответствующих солей:
CH 3 COONa + HCl → СН 3 СООН + NaCl .
Соли карбоновых кислот в водных растворах гидролизованы:
СН 3 СООК + Н 2 О
![]() СН 3 СООН + КОН.
СН 3 СООН + КОН.
Отличие карбоновых кислот от минеральных заключается в возможности образования ряда функциональных производных.
3 . Образование функциональных производных карбоновых кислот. При замещении группы ОН в карбоновых кислотах различными группами (/>X ) образуются функциональные производные кислот, имеющие общую формулу R -СО- X ; здесь R означает алкильную либо арильную группу. Хотя нитрилы имеют другую общую формулу ( R - CN ), обычно их также рассматривают как производные карбоновых кислот, поскольку они могут быть получены из этих кислот.
Хлорангидриды получают действием хлорида фосфора ( V ) на кислоты:
R-CO-OH + РС l 5 → R-CO-Cl + РОС l 3 + HCl .
|
Соединение примеры |
|
Кислота
Этановая(уксусная) Бензойная кислота хлорангидрит кислоты
Этаноилхлорид Бензоилхлорид (ацетилхлорид) ангидрид кислоты
Этановый(уксусный) бензойный ангидрит Ангидрит сложый эфир
Этилэтаноат(этилацетат) Метилбензоат амид Этанамид(ацетамид) Бензамид Нитрил Этаннитрил Бензонитрил (ацетонитрил) |
Ангидриды образуются из карбоновых кислот при действии водоотнимающих средств:
2 R — CO — OH + Р 2 О 5 → (R — CO -) 2 O + 2НРО 3 .
Сложные эфиры образуются при нагревании кислоты со спиртом в присутствии серной кислоты (обратимая реакция этерификации):
Механизм реакции этерификации был установлен методом "меченых атомов".
Сложные эфиры можно также получить при взаимодействии хлорангидридов кислот и алкоголятов щелочных металлов:
R-CO-Cl + Na-O-R’ → R-CO-OR’ + NaCl .
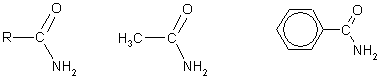
Реакции хлорангидридов карбоновых кислот с аммиаком приводят к образованию амидов :
СН 3 -СО-С l + CН 3 → СН 3 -СО-CН 2 + HCl .
Кроме того, амиды могут быть получены при нагревании аммонийных солей карбоновых кислот:
При нагревании амидов в присутствии водоотнимающих средств они дегидратируются с образованием нитрилов :
| Р 2 0 5 | ||
| CH 3 — CO — NH 2 |
→ |
CH 3 — C ≡ N + Н 2 О |
Функциональные производные низших кислот — летучие жидкости. Все они легко гидролизуются с образованием исходной кислоты:
R-CO-X + Н 2 О →R-CO-OH + НХ .
В кислой среде эти реакции могут быть обратимы. Гидролиз в щелочной среде необратим и приводит к образованию солей карбоновых кислот, например:
R-CO-OR ‘ + NaOH → R-CO-ONa + R’OH.
4 . Ряд свойств карбоновых кислот обусловлен наличием углеводородного радикала. Так, при действии галогенов на кислоты в присутствии красного фосфора образуются галогензамещенные кислоты, причем на галоген замещается атом водорода при соседнем с карбоксильной группой атоме углерода (а-атоме):/>
| р кр | ||
|
СН 3 -СН 2 -СООН + Вr 2 |
→ |
СН 3 -СНВr-СООН + НВr |
Непредельные карбоновые кислоты способны к реакциям присоединения:
СН 2 =СН-СООН + Н 2 → СН 3 -СН 2 -СООН,
СН 2 =СН-СООН + С l 2 → СН 2 С l -СНС l -СООН,
СН 2 =СН-СООН + HCl → СН 2 С l -СН 2 -СООН,
СН 2 =СН-СООН + Н 2 O → НО-СН 2 -СН 2 -СООН,
Две последние реакции протекают против правила Марковникова.
Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации .

5 . Окислительно-восстановительные реакции карбоновых кислот./>
Карбоновые кислоты при действии восстановителей в присутствии катализаторов способны превращаться в альдегиды, спирты и даже углеводороды:
Муравьиная кислота НСООН отличается рядом особенностей, поскольку в ее составе есть альдегидная группа:

Муравьиная кислота - сильный восстановитель и легко окисляется до СО 2 . Она дает реакцию "серебряного зеркала" :
НСООН + 2OH → 2Ag + (NH 4) 2 CO 3 + 2NH 3 + H 2 O,
или в упрощенном виде:
C Н 3 НСООН + Аg 2 О → 2Аg + СО 2 + Н 2 О.
Кроме того, муравьиная кислота окисляется хлором:
НСООН + Сl 2 → СО 2 + 2 HCl .
В атмосфере кислорода карбоновые кислоты окисляются до СО 2 и Н 2 О:
СН 3 СООН + 2О 2 → 2СО 2 + 2Н 2 О.
6 . Реакции декарбоксширования . Насыщенные незамещенные монокарбоновые кислоты из-за большой прочности связи С-С при нагревании декарбоксилируются с трудом. Для этого необходимо сплавление соли щелочного металла карбоновой кислоты со щелочью:/>
Появление электронодонорных заместителей в углеводородном радикале способствует реакции декарбоксилирования :
Двухосновные карбоновые кислоты легко отщепляют СО 2 при нагревании:
1. Гидролиз (кислотный и щелочной)
Проходит в наиболее жестких условиях, причем в отличие от всех производных кислот в один или два этапа, промежуточным соединениями являются амиды. При эквимольном соотношении нитрила и воды можно остановить реакцию на стадии образования амида. Обычно реакцию ведут с избытком воды, получают карбоновые кислоты (кислый гидролиз) или их соли (щелочной гидролиз) и аммиак.
а) кислый гидролиз








б) щелочной гидролиз
2. Алкоголиз нитрилов - синтез сложных эфиров. Реакция идет в два этапа через образование нестабильных иминоэфиров, гидролиз которых приводит к сложным эфирам

3. Восстановление нитрилов - синтез первичных аминов

Контрольные вопросы к главе «ОДНООСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ И ИХ ФУНКЦИОНАЛЬНЫЕ ПРОИЗВОДНЫЕ»
- 1. Напишите структурные формулы кислот: а) пропионовой; б) масляной; в) -метилмасляной; г) валериановой; д) капроновой. Назовите их по международной номенклатуре.
- 2. Приведите структурные формулы кислот: а) диметилпропановой; б) 3-метилбутановой; в) 4-метил-2-этилпентановой; г) 2,2,3-триметилбутановой; д) 3,5-диметил-4-этилгексановой. Дайте этим соединениям другие названия.
- 3. Какое строение имеют следующие кислоты: а) акриловая; б) кротоновая; в) винилуксусная? Назовите их по международной номенклатуре. Для какой кислоты возможна цис- и транс-изомерия?
- 4. Какую группу атомов называют кислотным остатком или ацилом? Приведите ацилы, соответствующие следующим кислотам: а) муравьиной; б) уксусной; в) пропионовой; г) масляной. Назовите их.
- 5. Обьясните, почему: а) уксусная кислота кипит при более высокой температуре, чем этиловый спирт (т.кип. 118C и 78C соответственно); б) низшие кислоты хорошо растворимы в воде; в) температура плавления щавелевой кислоты существенно выше, чем у уксусной кислоты (т.пл. 189C и 16,5C соответственно); г) дикарбоновые кислоты не обладают неприятным запахом, характерным для низкомолекулярных монокарбоновых кислот.
- 6. С помощью индуктивного и мезомерных эффектов обьясните влияние карбоксильной группы на углеводородный остаток в кислотах: а) пропионовой; б) акриловой; в) винилуксусной. Укажите в радикале наиболее активные атомы водорода, отметьте дробными зарядами распределение -электронной плотности.
- 7. Обьясните изменения кислотности в приведенных ниже рядах:

- 8. Какая кислота в каждой паре более сильная и почему: а) муравьиная и уксусная; б) уксусная и триметилуксусная; в) -хлормасляная и -хлормасляная; г) пропионовая и акриловая.
- 9. Напишите уравнения реакций пропионовой кислоты с указанными реагентами: а) Zn; б) NaOH; в) NaHСO3; г) NН4OH; д) Са(ОН)2. Какое свойство пропионовой кислоты проявляется в этих реакциях? Назовите полученные соединения. Какие из этих реакций применяются для качественного обнаружения карбоксильной группы в органических соединениях?



































- 10. Напишите схему этерификации пропионовой кислоты метиловым спиртом в присутствии серной кислоты. Приведите механизм.
- 11. Приведите схемы кислотного и щелочного гидролиза этилпропионата. Обьясните, почему щелочи катализируют только гидролиз сложных эфиров, но не их образование.
- 12. Напишите схемы реакций:

Назовите продукты. Что получится, если на образовавшиеся соединения подействовать этиловым спиртом, диметиламином? Приведите уравнения последних реакций, рассмотрите механизм одной из них.
13. Напишите схему и механизм реакции ацетата натрия с хлористым ацетилом, хлористым пропионилом. Что получится, если уксусный ангидрид нагреть с пропиловым спиртом? Приведите схему и механизм этого превращения.
14. Назовите соединения, являющиеся продуктами следующих реакций:

Сравните осномвные свойства продуктов с исходными аминами.
- 15. Какой химический процесс называют ацилированием? Приведите примеры реакций N- и О-ацилирования. Сопоставьте ацилирующую способность следующих соединений: а) СН3СН2СOOH; б) СН3СН2СОСl; в) СН3СН2СООСН3; г) (СН3СН2СО)2O; д) СН3СН2СОNН2. Какие функциональные произодные кислот являются наиболее сильными ацилирующими реагентами?
- 16. Напишите схему гидролиза производных масляной кислоты: а) хлорангидрида; б) ангидрида; в) сложного эфира; г) амида. Обьясните каталитическое действие кислот и оснований в этом процессе.
- 17. Какие соединения образуются при действии на этилацетат следующих реагентов: а) Н2О (Н+); б) Н2О (NaOH); в) СН3ОН (Н+); г) СН3СН2СН2ОН (кат. RO); д) NН3, t; e) LiAlН4 (эфир), затем Н2О? Приведите полные уравнения реакций.
- 18. Сравните основные и кислотные свойства соединений: а) этиламина; б) ацетамида; в) N,N-диметиацетамида. Дайте обьяснения имеющимся отличиям. Напишите реакции этих соединений с HCl в эфире и NaNН2 в NН3, если есть взаимодействие.
- 19. Назовите соединения, образующиеся из амида масляной кислоты со следующими реагентами: а) Н2О (Н+); б) Br2+KOH; в) LiAlH4 (эфир), затем Н2О; г) Р2О5 , t; д) НNO2 (Н2О).
- 20. Напишите схемы взаимодействия нитрила изомасляной кислоты с указанными реагентами: а) Н2О, Н+, t; б) CН3СН2MgBr, затем Н2О; в) LiAlН4. Назовите продукты реакций.
- 21. Напишите реакции акриловой кислоты со следующими соединениями: а) Na2СO3; б) СН3СН2ОН (Н+); в) SOСl2; г) НBr; д) Br2. Приведите механизм реакции с HBr.
- 22. Для каждой пары соединений приведите химическую реакцию, позволяющие отличить эти соединения: а) НСООН и СН3СООН; б) СН3СООН и СН3СООС2Н5; в) СН3СН2СООН и СН2=СНCOOH; г) СН2=СНCOOH и НС?СCOOH; д) СН3СОN(СН3)2 и (СН3СН2)3N; е) СН3СОNН2 и СН3СООNН4.

23. Напишите уравнения реакций. Назовите исходные и конечные соединения:

24. Назовите кислоты, являющиеся продуктами следующих реакций:

- 25. Приведите схемы получения изомасляной кислоты из соответствующих соединений указанными методами: а) окислением спирта; б) гидролизом нитрила; в) реакцией Гриньяра; г) алкилированием малонового эфира.
- 26. Получите пропионовую кислоту из следующих соединений: а) пропанола-1; б) пропена; в) бромистого этила.
- 27. Напишите схемы получения из пропионовой кислоты её производных: а) натриевой соли; б) кальциевой соли; в) хлорангидрида; г) амида; д) нитрила; е) ангидрида; ж) этилового эфира.
- 28. Назовите соединения и приведите схемы их синтеза из соответствующих кислот: а) СН3СН2СООСН3; б) (СН3)2СНСОNН2; в) СН3СН2СН2СN.

29. Заполните схемы превращений. Назовите все полученные соединения:


1. Гидролиз (кислотный и щелочной)
Проходит в наиболее жестких условиях, причем в отличие от всех производных кислот в один или два этапа, промежуточным соединениями являются амиды. При эквимольном соотношении нитрила и воды можно остановить реакцию на стадии образования амида. Обычно реакцию ведут с избытком воды, получают карбоновые кислоты (кислый гидролиз) или их соли (щелочной гидролиз) и аммиак.
а) кислый гидролиз
б) щелочной гидролиз
2. Алкоголиз нитрилов – синтез сложных эфиров. Реакция идет в два этапа через образование нестабильных иминоэфиров, гидролиз которых приводит к сложным эфирам.

3. Восстановление нитрилов – синтез первичных аминов.
![]()
Контрольные вопросы к главе «ОДНООСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ И ИХ ФУНКЦИОНАЛЬНЫЕ ПРОИЗВОДНЫЕ»
1. Напишите структурные формулы кислот: а) пропионовой; б) масляной; в) -метилмасляной; г) валериановой; д) капроновой. Назовите их по международной номенклатуре.
2. Приведите структурные формулы кислот: а) диметилпропановой; б) 3-метилбутановой; в) 4-метил-2-этилпентановой; г) 2,2,3-триметилбутановой; д) 3,5-диметил-4-этилгексановой. Дайте этим соединениям другие названия.
3. Какое строение имеют следующие кислоты: а) акриловая; б) кротоновая; в) винилуксусная? Назовите их по международной номенклатуре. Для какой кислоты возможна цис - итранс- изомерия?
4. Какую группу атомов называют кислотным остатком или ацилом? Приведите ацилы, соответствующие следующим кислотам: а) муравьиной; б) уксусной; в) пропионовой; г) масляной. Назовите их.
5. Обьясните, почему: а) уксусная кислота кипит при более высокой температуре, чем этиловый спирт (т.кип. 118C и 78C соответственно); б) низшие кислоты хорошо растворимы в воде; в) температура плавления щавелевой кислоты существенно выше, чем у уксусной кислоты (т.пл. 189C и 16,5C соответственно); г) дикарбоновые кислоты не обладают неприятным запахом, характерным для низкомолекулярных монокарбоновых кислот.
6. С помощью индуктивного и мезомерных эффектов обьясните влияние карбоксильной группы на углеводородный остаток в кислотах: а) пропионовой; б) акриловой; в) винилуксусной. Укажите в радикале наиболее активные атомы водорода, отметьте дробными зарядами распределение -электронной плотности.
7. Обьясните изменения кислотности в приведенных ниже рядах:

8. Какая кислота в каждой паре более сильная и почему: а) муравьиная и уксусная; б) уксусная и триметилуксусная; в) -хлормасляная и-хлормасляная; г) пропионовая и акриловая.
9. Напишите уравнения реакций пропионовой кислоты с указанными реагентами: а) Zn; б) NaOH; в) NaHСO 3 ; г) NН 4 OH; д) Са(ОН) 2 . Какое свойство пропионовой кислоты проявляется в этих реакциях? Назовите полученные соединения. Какие из этих реакций применяются для качественного обнаружения карбоксильной группы в органических соединениях?
10. Напишите схему этерификации пропионовой кислоты метиловым спиртом в присутствии серной кислоты. Приведите механизм.
11. Приведите схемы кислотного и щелочного гидролиза этилпропионата. Обьясните, почему щелочи катализируют только гидролиз сложных эфиров, но не их образование.
12. Напишите схемы реакций:
![]()
Назовите продукты. Что получится, если на образовавшиеся соединения подействовать этиловым спиртом, диметиламином? Приведите уравнения последних реакций, рассмотрите механизм одной из них.
13. Напишите схему и механизм реакции ацетата натрия с хлористым ацетилом, хлористым пропионилом. Что получится, если уксусный ангидрид нагреть с пропиловым спиртом? Приведите схему и механизм этого превращения.
14. Назовите соединения, являющиеся продуктами следующих реакций:
![]()
Сравните осно́вные свойства продуктов с исходными аминами.
15. Какой химический процесс называют ацилированием? Приведите примеры реакций N- и О-ацилирования. Сопоставьте ацилирующую способность следующих соединений: а) СН 3 СН 2 СOOH; б) СН 3 СН 2 СОСl; в) СН 3 СН 2 СООСН 3 ; г) (СН 3 СН 2 СО) 2 O; д) СН 3 СН 2 СОNН 2 . Какие функциональные произодные кислот являются наиболее сильными ацилирующими реагентами?
16. Напишите схему гидролиза производных масляной кислоты: а) хлорангидрида; б) ангидрида; в) сложного эфира; г) амида. Обьясните каталитическое действие кислот и оснований в этом процессе.
17. Какие соединения образуются при действии на этилацетат следующих реагентов: а) Н 2 О (Н + ); б) Н 2 О (NaOH); в) СН 3 ОН (Н + ); г) СН 3 СН 2 СН 2 ОН (кат. RO); д) NН 3 , t ; e) LiAlН 4 (эфир), затем Н 2 О? Приведите полные уравнения реакций.
18. Сравните основные и кислотные свойства соединений: а) этиламина; б) ацетамида; в) N,N -диметиацетамида. Дайте обьяснения имеющимся отличиям. Напишите реакции этих соединений сHCl в эфире иNaNН 2 вNН 3 , если есть взаимодействие.
19. Назовите соединения, образующиеся из амида масляной кислоты со следующими реагентами: а) Н 2 О (Н + ); б) Br 2 +KOH; в) LiAlH 4 (эфир), затем Н 2 О; г) Р 2 О 5 , t ; д) НNO 2 (Н 2 О).
20.Напишите схемы взаимодействия нитрила изомасляной кислоты с указанными реагентами: а) Н 2 О, Н + , t ; б) CН 3 СН 2 MgBr, затем Н 2 О; в) LiAlН 4 . Назовите продукты реакций.
21. Напишите реакции акриловой кислоты со следующими соединениями: а) Na 2 СO 3 ; б) СН 3 СН 2 ОН (Н + ); в) SOСl 2 ; г) НBr; д) Br 2 . Приведите механизм реакции сHBr .
22. Для каждой пары соединений приведите химическую реакцию, позволяющие отличить эти соединения: а) НСООН и СН 3 СООН; б) СН 3 СООН и СН 3 СООС 2 Н 5 ; в) СН 3 СН 2 СООН и СН 2 =СНCOOH; г) СН 2 =СНCOOH и НС ≡ СCOOH; д) СН 3 СОN(СН 3 ) 2 и (СН 3 СН 2 ) 3 N; е) СН 3 СОNН 2 и СН 3 СООNН 4 .
23. Напишите уравнения реакций. Назовите исходные и конечные соединения:

24. Назовите кислоты, являющиеся продуктами следующих реакций:

25. Приведите схемы получения изомасляной кислоты из соответствующих соединений указанными методами: а) окислением спирта; б) гидролизом нитрила; в) реакцией Гриньяра; г) алкилированием малонового эфира.
26. Получите пропионовую кислоту из следующих соединений: а) пропанола-1; б) пропена; в) бромистого этила.
27. Напишите схемы получения из пропионовой кислоты её производных: а) натриевой соли; б) кальциевой соли; в) хлорангидрида; г) амида; д) нитрила; е) ангидрида; ж) этилового эфира.
28. Назовите соединения и приведите схемы их синтеза из соответствующих кислот: а) СН 3 СН 2 СООСН 3 ; б) (СН 3 ) 2 СНСОNН 2 ; в) СН 3 СН 2 СН 2 СN .
29. Заполните схемы превращений. Назовите все полученные соединения:

30. Действием каких реагентов и в каких условиях можно осуществить указанные превращения (все соединения назовите).
Материал из Википедии - свободной энциклопедии
Нитри́лы - органические соединения общей формулы R-C≡N, формально являющиеся C-замещенными производными синильной кислоты HC≡N .
Номенклатура
Нитрилы также часто рассматривают как производные карбоновых кислот (продукты дегидратации амидов) и именуют как производные соответствующих карбоновых кислот, например, CH 3 C≡N - ацетонитрил (нитрил уксусной кислоты), C 6 H 5 CN - бензонитрил (нитрил бензойной кислоты). В систематической номенклатуре для именования нитрилов используется суффикс карбонитрил , например, пиррол-3-карбонитрил.
Нитрилы, в которых группа -C≡N подвижна либо имеет псевдогалогенный характер обычно называют цианидами, например, C 6 H 5 CH 2 CN - бензилцианид, C 6 H 5 COCN - бензоилцианид, (CH 3) 3 SiCN - триметилсилилцианид.
Строение нитрильной группы
Атомы азота и углерода в нитрильной группе находятся в состоянии sp-гибридизации. Длина тройной связи C≡N составляет 0,116 нм, длина связи R-CN 0,1468 нм (для CH 3 CN). Нитрильная группа обладает отрицательными мезомерным и индукционным эффектами, в частности, константы Гаммета σ M = 0,56; σ n = 0,66; σ n - = 1,00; σ n + = 0,659, а индуктивная константа Тафта σ * = 3,6.
Электронное строение нитрилов можно изобразить в виде двух резонансных структур:
В ИК-спектрах и спектрах комбинационного рассеяния нитрильная группа имеет полосу поглощения в районе 2220-2270 см -1 .
Физические и химические свойства
Нитрилы являются жидкими или твёрдыми веществами. Они растворяются в органических растворителях. Низшие нитрилы хорошо растворяются в воде, но с увеличением их молярной массы растворимость в воде падает.
Нитрилы способны вступать в реакции как с электрофильными реагентами по атому азота, так и с нуклеофильными реагентами по атому углерода, что обусловлено резонансной структурой нитрильной группы. Неподелённая электронная пара на атоме азота способствует образованию комплексов нитрилов с солями металлов, например, с CuCl, NiCl 2 , SbCl 5 . Наличие нитрильной группы приводит к снижению энергии диссоциации связи C-H у α-углеродного атома. Связь C≡N способна присоединять другие атомы и группы.
Гидролиз нитрилов в щелочной среде даёт соли карбоновых кислот.
При действии на нитрилы сероводорода образуются тиоамиды RC(S)NH 2 , при действии аммиака, первичных и вторичных аминов - амидины RC(NHR")=NH, при действии гидроксиламина - амидоксимы RC(NH 2)=NOH, при действии гидразона - амидогидразоны RC(NH 2)=NNH 2 .
Нитрилы реагируют с ненасыщенными соединениями (реакция Риттера) с образованием замещённых амидов:
Восстановление нитрилов идёт постадийно до образования первичных аминов . Чаще всего реакцию проводят водородом на платиновом, палладиевом (при 1-3 атм. 20-50 °C) или никелевом, кобальтовом катализаторах (100-250 атм., 100-200 °C) в присутствии аммиака. В лабораторных условиях нитрилы восстанавливают натрием в этаноле , алюмогидридом калия и борогидридом натрия :
Реакция нитрилов с карбонильными соединениями по Кнёвенагелю ведёт к цианоалкенам:
Получение
Нитрилы получают следующими способами:
Дегидратацией амидов, альдоксимов, аммониевых солей карбоновых кислот Алкилированием солей синильной кислоты По реакции Зандмейера Присоединением синильной кислоты (используется в промышленности) Совместным окислением аммиака и углеводородов (окислительный аммонолиз)
Реакция протекает при 400-500 °C, катализаторами служат молибдаты и фосфомолибдаты висмута , молибдаты и вольфраматы церия и др.:
Окислением аминов
Воздействие на организм человека
Нитрилы ядовиты для человека вследствие нарушения действия цитохромоксидазы и угнетения функции переноса кислорода из крови к клеткам. Токсическое действие проявляется как при вдыхании паров нитрилов, так и при попадании в организм через кожу или желудочно-кишечный тракт.
Токсичность нитрилов увеличивается с ростом длины углеводородного радикала и степени разветвлённости углеродной цепи. Ненасыщенные нитрилы токсичнее, чем насыщенные.
Применение
Нитрилы используются в качестве растворителей, инициаторов радикально-цепной полимеризации , сырья для получения мономеров, лекарственных средств, пестицидов , пластификаторов. Имеют широкое применение в реакции Риттера как нуклеофильный реагент.
Напишите отзыв о статье "Нитрилы"
Примечания
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. - М .: Советская энциклопедия, 1992. - Т. 3 (Мед-Пол). - 639 с. - ISBN 5-82270-039-8 .
- О. Я. Нейланд. Органическая химия. - М .: Высшая школа, 1990. - 751 с. - 35 000 экз. - ISBN 5-06-001471-1 .
- Зильберман Е.Н. Реакции нитрилов. - Москва: Химия, 1972. - 448 с.
- Новый справочник химика и технолога. Радиоактивные вещества. Вредные вещества. Гигиенические нормативы / Редкол.: Москвин А. В. и др.. - СПб. : АНО НПО «Профессионал», 2004. - 1142 с.
См. также
|
||||||||||||||||||||||||||||||||||||||
Отрывок, характеризующий Нитрилы
Как только Наташа, сидевшая у изголовья князя Андрея, узнала о приезде княжны Марьи, она тихо вышла из его комнаты теми быстрыми, как показалось княжне Марье, как будто веселыми шагами и побежала к ней.На взволнованном лице ее, когда она вбежала в комнату, было только одно выражение – выражение любви, беспредельной любви к нему, к ней, ко всему тому, что было близко любимому человеку, выраженье жалости, страданья за других и страстного желанья отдать себя всю для того, чтобы помочь им. Видно было, что в эту минуту ни одной мысли о себе, о своих отношениях к нему не было в душе Наташи.
Чуткая княжна Марья с первого взгляда на лицо Наташи поняла все это и с горестным наслаждением плакала на ее плече.
– Пойдемте, пойдемте к нему, Мари, – проговорила Наташа, отводя ее в другую комнату.
Княжна Марья подняла лицо, отерла глаза и обратилась к Наташе. Она чувствовала, что от нее она все поймет и узнает.
– Что… – начала она вопрос, но вдруг остановилась. Она почувствовала, что словами нельзя ни спросить, ни ответить. Лицо и глаза Наташи должны были сказать все яснее и глубже.
Наташа смотрела на нее, но, казалось, была в страхе и сомнении – сказать или не сказать все то, что она знала; она как будто почувствовала, что перед этими лучистыми глазами, проникавшими в самую глубь ее сердца, нельзя не сказать всю, всю истину, какою она ее видела. Губа Наташи вдруг дрогнула, уродливые морщины образовались вокруг ее рта, и она, зарыдав, закрыла лицо руками.
Княжна Марья поняла все.
Но она все таки надеялась и спросила словами, в которые она не верила:
– Но как его рана? Вообще в каком он положении?
– Вы, вы… увидите, – только могла сказать Наташа.
Они посидели несколько времени внизу подле его комнаты, с тем чтобы перестать плакать и войти к нему с спокойными лицами.
– Как шла вся болезнь? Давно ли ему стало хуже? Когда это случилось? – спрашивала княжна Марья.
Наташа рассказывала, что первое время была опасность от горячечного состояния и от страданий, но в Троице это прошло, и доктор боялся одного – антонова огня. Но и эта опасность миновалась. Когда приехали в Ярославль, рана стала гноиться (Наташа знала все, что касалось нагноения и т. п.), и доктор говорил, что нагноение может пойти правильно. Сделалась лихорадка. Доктор говорил, что лихорадка эта не так опасна.
– Но два дня тому назад, – начала Наташа, – вдруг это сделалось… – Она удержала рыданья. – Я не знаю отчего, но вы увидите, какой он стал.
– Ослабел? похудел?.. – спрашивала княжна.
– Нет, не то, но хуже. Вы увидите. Ах, Мари, Мари, он слишком хорош, он не может, не может жить… потому что…
Когда Наташа привычным движением отворила его дверь, пропуская вперед себя княжну, княжна Марья чувствовала уже в горле своем готовые рыданья. Сколько она ни готовилась, ни старалась успокоиться, она знала, что не в силах будет без слез увидать его.
Княжна Марья понимала то, что разумела Наташа словами: сним случилось это два дня тому назад. Она понимала, что это означало то, что он вдруг смягчился, и что смягчение, умиление эти были признаками смерти. Она, подходя к двери, уже видела в воображении своем то лицо Андрюши, которое она знала с детства, нежное, кроткое, умиленное, которое так редко бывало у него и потому так сильно всегда на нее действовало. Она знала, что он скажет ей тихие, нежные слова, как те, которые сказал ей отец перед смертью, и что она не вынесет этого и разрыдается над ним. Но, рано ли, поздно ли, это должно было быть, и она вошла в комнату. Рыдания все ближе и ближе подступали ей к горлу, в то время как она своими близорукими глазами яснее и яснее различала его форму и отыскивала его черты, и вот она увидала его лицо и встретилась с ним взглядом.
Он лежал на диване, обложенный подушками, в меховом беличьем халате. Он был худ и бледен. Одна худая, прозрачно белая рука его держала платок, другою он, тихими движениями пальцев, трогал тонкие отросшие усы. Глаза его смотрели на входивших.
Увидав его лицо и встретившись с ним взглядом, княжна Марья вдруг умерила быстроту своего шага и почувствовала, что слезы вдруг пересохли и рыдания остановились. Уловив выражение его лица и взгляда, она вдруг оробела и почувствовала себя виноватой.
«Да в чем же я виновата?» – спросила она себя. «В том, что живешь и думаешь о живом, а я!..» – отвечал его холодный, строгий взгляд.
В глубоком, не из себя, но в себя смотревшем взгляде была почти враждебность, когда он медленно оглянул сестру и Наташу.
Он поцеловался с сестрой рука в руку, по их привычке.
– Здравствуй, Мари, как это ты добралась? – сказал он голосом таким же ровным и чуждым, каким был его взгляд. Ежели бы он завизжал отчаянным криком, то этот крик менее бы ужаснул княжну Марью, чем звук этого голоса.
– И Николушку привезла? – сказал он также ровно и медленно и с очевидным усилием воспоминанья.
– Как твое здоровье теперь? – говорила княжна Марья, сама удивляясь тому, что она говорила.
– Это, мой друг, у доктора спрашивать надо, – сказал он, и, видимо сделав еще усилие, чтобы быть ласковым, он сказал одним ртом (видно было, что он вовсе не думал того, что говорил): – Merci, chere amie, d"etre venue. [Спасибо, милый друг, что приехала.]
Княжна Марья пожала его руку. Он чуть заметно поморщился от пожатия ее руки. Он молчал, и она не знала, что говорить. Она поняла то, что случилось с ним за два дня. В словах, в тоне его, в особенности во взгляде этом – холодном, почти враждебном взгляде – чувствовалась страшная для живого человека отчужденность от всего мирского. Он, видимо, с трудом понимал теперь все живое; но вместе с тем чувствовалось, что он не понимал живого не потому, чтобы он был лишен силы понимания, но потому, что он понимал что то другое, такое, чего не понимали и не могли понять живые и что поглощало его всего.
– Да, вот как странно судьба свела нас! – сказал он, прерывая молчание и указывая на Наташу. – Она все ходит за мной.
Княжна Марья слушала и не понимала того, что он говорил. Он, чуткий, нежный князь Андрей, как мог он говорить это при той, которую он любил и которая его любила! Ежели бы он думал жить, то не таким холодно оскорбительным тоном он сказал бы это. Ежели бы он не знал, что умрет, то как же ему не жалко было ее, как он мог при ней говорить это! Одно объяснение только могло быть этому, это то, что ему было все равно, и все равно оттого, что что то другое, важнейшее, было открыто ему.
Разговор был холодный, несвязный и прерывался беспрестанно.
– Мари проехала через Рязань, – сказала Наташа. Князь Андрей не заметил, что она называла его сестру Мари. А Наташа, при нем назвав ее так, в первый раз сама это заметила.
– Ну что же? – сказал он.
– Ей рассказывали, что Москва вся сгорела, совершенно, что будто бы…
Наташа остановилась: нельзя было говорить. Он, очевидно, делал усилия, чтобы слушать, и все таки не мог.
– Да, сгорела, говорят, – сказал он. – Это очень жалко, – и он стал смотреть вперед, пальцами рассеянно расправляя усы.
– А ты встретилась с графом Николаем, Мари? – сказал вдруг князь Андрей, видимо желая сделать им приятное. – Он писал сюда, что ты ему очень полюбилась, – продолжал он просто, спокойно, видимо не в силах понимать всего того сложного значения, которое имели его слова для живых людей. – Ежели бы ты его полюбила тоже, то было бы очень хорошо… чтобы вы женились, – прибавил он несколько скорее, как бы обрадованный словами, которые он долго искал и нашел наконец. Княжна Марья слышала его слова, но они не имели для нее никакого другого значения, кроме того, что они доказывали то, как страшно далек он был теперь от всего живого.
приводит к образованию



Восстановление амидов .
абс. эфир
абс. эфир
Образование сложных эфиров
Перегруппировка Гофмана
й
Нитрилы
Определение.
Номенклатура. По номенклатуре IUPAC название нитрилов карбоновых кислот образуют, добавляя суффикс «нитрил» к названию родоначального углеводорода с тем же числом атомов углерода. Нитрилы также называют как производные кислот, заменяя в названии «-карбоновая кислота» на «-карбо-нитрил». Название нитрила от тривиального названия кислоты образуется путем замены суффикса «-оил» (или «-ил») на «-онитрил». Нитрилы можно рассматривать как производные синильной кислоты и называть алкил- или арилцианиды.
Способы получения
: R–Br + KCN ¾¾® R–CN + KBr

R–CH=N–OH ¾¾¾® R–C≡N + Н2О
:
Химические свойства.
Гидролиз нитрилов в кислой сред е

несколько стадий

Алкоголиз
Восстановление
R–C≡N + H2 ¾¾® R–CH2–NH2
ПОСМОТРЕТЬ ЕЩЕ:
Химические свойства
К основнымхимическим реакциям амидов относятся гидролиз в кислой и щелочной среде, восстановление, дегидратация при нагревании с водоотнимающими средствами и перегруппировка Гофмана.
Гидролиз амидов в кислой или щелочной среде приводит к образованию
образованию карбоновых кислот или их солей соответственно. Механизм гидролиза амидов в кислой среде следующий:

Механизм гидролиза амидов в щелочной среде:


Восстановление амидов . При восстановлении амидов карбоновых кислот алюмогидридом лития образуются первичные амины, в случае N-замещенных или N,N-дизамещенных амидов – вторичные или третичные амины соответственно:
абс. эфир
абс. эфир
Образование сложных эфиров при взаимодействии со спиртами в присутствии минеральных кислот:
Дегидратация первичных амидов карбоновых кислот при нагревании с водоотнимающими реагентами с образованием нитрилов:
Перегруппировка Гофмана под действием гипогалогенидов из первичных амидов с получением первичных аминов:
Взаимодействие первичных амидов с азотистой кислото й с выделением карбоновых кислот и азота:
Нитрилы
Определение. Нитрилами называются соединения с формулой R–C≡N.
Номенклатура. По номенклатуре IUPAC название нитрилов карбоновых кислот образуют, добавляя суффикс «нитрил» к названию родоначального углеводорода с тем же числом атомов углерода.
Ангидриды карбоновых кислот. Кетены. Нитрилы
Нитрилы также называют как производные кислот, заменяя в названии «-карбоновая кислота» на «-карбо-нитрил». Название нитрила от тривиального названия кислоты образуется путем замены суффикса «-оил» (или «-ил») на «-онитрил». Нитрилы можно рассматривать как производные синильной кислоты и называть алкил- или арилцианиды.
этанонитрил, ацетонитрил, фенилацетонитрил, циклогексаекарбонитрил,
метилцианид, нитрил бензилцианид, нитрил нитрил циклогексан-
пропионовой кислоты фенилуксусной кислоты карбоновой кислоты
Способы получения
Взаимодействие галогенопроизводных углеводородов с цианидами щелочных металлов : R–Br + KCN ¾¾® R–CN + KBr
Дегидратация амидов карбоновых кислот при нагревании с водоотнимающими реагентами, например, Р2О5:

Аналогично подвергаются дегидратации оксимы альдегидов:
R–CH=N–OH ¾¾¾® R–C≡N + Н2О
Нитрилы ароматических кислот можно получать в результате сплавления солей ароматических сульфокислот с цианидами щелочных металлов :
Химические свойства. Для нитрилов характерны реакции гидролиза в кислой или щелочной среде и реакции восстановления.
Гидролиз нитрилов в кислой сред е обеспечивает получение карбоновых кислот с образованием амидов как промежуточных продуктов реакции:

несколько стадий
Гидролиз нитрилов в щелочной среде заканчивается образованием солей карбоновых кислот:

Алкоголиз нитрилов приводит к сложным эфирам:
R–C≡N + R’–OH + H2O ¾¾® R–COOR’ + NH3
Восстановление нитрилов приводит к получению первичных аминов:
R–C≡N + H2 ¾¾® R–CH2–NH2
ПОСМОТРЕТЬ ЕЩЕ:
Общая формула

Классификация
(т. е. числукарбоксильных групп в молекуле):
(монокарбоновые) RCOOH; например:
СН3СН2СН2СООН;
НООС-СН2-СООН пропандиовая (малоновая) кислота

(трикарбоновые) R(COOH)3 и т.
Химические свойства
предельные; например: СН3СН2СООН;
непредельные; например: СН2=СНСООН пропеновая(акриловая) кислота

Например:

Например:

Предельные монокарбоновые кислоты
(одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой -COOH. Все они имеют общую формулу
Номенклатура
Систематические названия одноосновных предельных карбоновых кислот даются по названию соответствующего с добавлением суффикса — и слова
1. НСООН метановая (муравьиная) кислота
2. СН3СООН этановая (уксусная) кислота
3. СН3СН2СООН пропановая (пропионовая) кислота
Изомерия
Изомерия скелета в углеводородном радикале проявляется, начиная с бутановой кислоты, которая имеет два изомера:

Межклассовая изомерия проявляется, начиная с уксусной кислоты:
— CH3-COOH уксусная кислота;
— H-COO-CH3 метилформиат (метиловый эфир муравьиной кислоты);
— HO-CH2-COH гидроксиэтаналь (гидроксиуксусный альдегид);
— HO-CHO-CH2 гидроксиэтиленоксид.
Гомологический ряд
|
Тривиальное название |
Название по ИЮПАК |
|
|
Муравьиная кислота |
Метановая кислота |
|
|
Уксусная кислота |
Этановая кислота |
|
|
Пропионовая кислота |
Пропановая кислота |
|
|
Масляная кислота |
Бутановая кислота |
|
|
Валериановая кислота |
Пентановая кислота |
|
|
Капроновая кислота |
Гексановая кислота |
|
|
Энантовая кислота |
Гептановая кислота |
|
|
Каприловая кислота |
Октановая кислота |
|
|
Пеларгоновая кислота |
Нонановая кислота |
|
|
Каприновая кислота |
Декановая кислота |
|
|
Ундециловая кислота |
Ундекановая кислота |
|
|
Пальмитиновая кислота |
Гексадекановая кислота |
|
|
Стеариновая кислота |
Октадекановая кислота |
Кислотные остатки и кислотные радикалы
|
Кислотный остаток |
Кислотный радикал (ацил) |
|
|
НСООН |
НСОО- |
|
|
СН3СООН |
СН3СОО- |
|
|
СН3СН2СООН |
СН3СН2СОО- |
|
|
СН3(СН2)2СООН |
СН3(СН2)2СОО- |
|
|
СН3(СН2)3СООН |
СН3(СН2)3СОО- |
|
|
СН3(СН2)4СООН |
СН3(СН2)4СОО- |
Электронное строение молекул карбоновых кислот

Показанное в формуле смещение электронной плотности в сторону карбонильного атома кислорода обусловливает сильную поляризацию связи О-Н, в результате чего облегчается отрыв атома водорода в виде протона — в водных растворах происходит процесс кислотной диссоциации:
RCOOH ↔ RCOO- + Н+
В карбоксилат-ионе (RCOO-) имеет место р, π-сопряжение неподеленной пары электронов атома кислорода гидроксильной группы с р-облаками, образующими π- связь, в результате происходит делокализация π- связи и равномерное распределение отрицательного заряда между двумя атомами кислорода:

В связи с этим для карбоновых кислот, в отличие от альдегидов, не характерны реакции присоединения.
Физические свойства

Температуры кипения кислот значительно выше температур кипения спиртов и альдегидов с тем же числом атомов углерода, что объясняется образованием циклических и линейных ассоциатов между молекулами кислот за счет водородных связей:
Химические свойства
I. Кислотные свойства
Сила кислот уменьшается в ряду:
НСООН → СН3СООН → C2H6COOH → …
1. Реакции нейтрализации
СН3СООН + КОН → СН3СООК + н2O
2. Реакции с основными оксидами
2HCOOH + СаО → (НСОО)2Са + Н2O
3. Реакции с металлами
2СН3СН2СООН + 2Na → 2СН3СН2COONa + H2
4. Реакции с солями более слабых кислот (в т. ч. с карбонатами и гидрокарбонатами)
2СН3СООН + Na2CO3 → 2CH3COONa + CO2 + Н2O
2НСООН + Mg(HCO3)2 → (НСОО)2Мg + 2СO2 + 2Н2O
(НСООН + НСО3- → НСОО- + СO2 +Н2O)
5. Реакции с аммиаком
СН3СООН + NH3 → CH3COONH4
II. Замещение группы -ОН
1. Взаимодействие со спиртами (реакции этерификации)

2. Взаимодействие с NH3 при нагревании (образуются амиды кислот)

Амиды кислот  гидролизуются с образованием кислот:
гидролизуются с образованием кислот:

или их солей:

3. Образование галогенангидридов
Наибольшее значение имеют. Хлорирующие реагенты — PCl3, PCl5, тионилхлорид SOCl2.

4. Образование ангидридов кислот (межмолекулярная дегидратация)

Ангидриды кислот образуются также при взаимодействии хлорангидридов кислот с безводными солями карбоновых кислот; при этом можно получать смешанные ангидриды различных кислот; например:


Особенности строения и свойств муравьиной кислоты
Строение молекулы

Молекула муравьиной кислоты, в отличие от других карбоновых кислот, содержит в своей структуре
Химические свойства
Муравьиная кислота вступает в реакции, характерные как для кислот, так и для альдегидов. Проявляя свойства альдегида, она легко окисляется до угольной кислоты:
В частности, НСООН окисляется аммиачным раствором Ag2O и гидроксидом меди (II) Сu(ОН)2, т. е. дает качественные реакции на альдегидную группу:

При нагревании с концентрированной H2SO4 муравьиная кислота разлагается на оксид углерода (II) и воду:

Муравьиная кислота заметно сильнее других алифатических кислот, так как карбоксильная группа в ней связана с атомом водорода, а не с электроно-донорным алкильным радикалом.
Способы получения предельных монокарбоновых кислот
1. Окисление спиртов и альдегидов
Общая схема окисления спиртов и альдегидов:
В качестве окислителей используют KMnO4, K2Cr2O7, HNO3 и другие реагенты.
Например:
5С2Н5ОН + 4KMnO4 + 6H2S04 → 5СН3СООН + 2K2SO4 + 4MnSO4 + 11Н2O
2. Гидролиз сложных эфиров

3. Окислительное расщепление двойных и тройных связей в алкенах и в алкинах

Способы получения НСООН (специфические)
1. Взаимодействие оксида углерода (II) с гидроксидом натрия
СO + NaOH → HCOONa формиат натрия
2HCOONa + H2SO4 → 2НСООН + Na2SO4
2. Декарбоксилирование щавелевой кислоты

Способы получения СН3СООН (специфические)
1. Каталитическое окисление бутана

2. Синтез из ацетилена

3. Каталитическое карбонилирование метанола

4. Уксуснокислое брожение этанола
Так получают пищевую уксусную кислоту.
Получение высших карбоновых кислот
Гидролиз природных жиров

Непредельные монокарбоновые кислоты
Важнейшие представители
Общая формула алкеновых кислот:
CH2=CH-COOH пропеновая (акриловая) кислота

Высшие непредельные кислоты
Радикалы этих кислот входят в состав растительных масел.
C17H33COOH — олеиновая кислота, или цис-октадиен-9-овая кислота

Транс-изомер олеиновой кислоты называется элаидиновой кислотой.
C17H31COOH — линолевая кислота, или цис, цис-октадиен-9,12-овая кислота

C17H29COOH — линоленовая кислота, или цис, цис, цис-октадекатриен-9,12,15-овая кислота
Кроме общих свойств карбоновых кислот, для непредельных кислот характерны реакции присоединения по кратным связям в углеводородном радикале. Так, непредельные кислоты, как и алкены, гидрируются и обесцвечивают бромную воду, например:

Отдельные представители дикарбоновых кислот
Предельные дикарбоновые кислоты HOOC-R-COOH
HOOC-CH2-COOH пропандиовая (малоновая) кислота, (соли и эфиры — малонаты)
HOOC-(CH2)2-COOH бутадиовая (янтарная) кислота, (соли и эфиры — сукцинаты)
HOOC-(CH2)3-COOH пентадиовая (глутаровая) кислота, (соли и эфиры — глутораты)
HOOC-(CH2)4-COOH гексадиовая (адипиновая) кислота, (соли и эфиры — адипинаты)
Особенности химических свойств
Дикарбоновые кислоты во многом сходны с монокарбоновыми, однако являются более сильными. Например, щавелевая кислотасильнее уксусной почти в 200 раз.
Дикарбоновые кислоты ведут себя как двухосновные и образуют два ряда солей — кислые и средние:
HOOC-COOH + NaOH → HOOC-COONa + H2O
HOOC-COOH + 2NaOH → NaOOC-COONa + 2H2O
При нагревании щавелевая и малоновая кислоты легко декарбоксилируются:

Амиды R-СОNН2 – производные карбоновых кислот, в которых гидроксильная группа -ОН замещена на аминогруппу -NH2 . Названия их строят из слова амид с добавлением названия соответствующей кислоты.
Нитрилы карбоновых кислот
Пример: амид уксусной кислоты CH 3 -СОNН 2 (ацетамид).
Амиды получают при взаимодействии кислот с аммиаком при нагревании для разложения образующейся аммониевой соли:
Водные растворы амидов дают нейтральную реакцию на лакмус, что отражает отсутствие основности (способности присоединять Н +) у атома азота, связанного с электроноакцепторной группой C=O.
Амиды гидролизуются в присутствии кислот (или оснований) с образованием соответствующей карбоновой кислоты (или её соли):
Мочевина – конечный продукт азотистого обмена в организме человека и животных, образующийся при распаде белков и выделяемый вместе с мочой.
Важную роль в природе играют полимерные амиды, к которым относятся белки. Молекулы белков построены из остатков -аминокислот с участием амидных групп – пептидных связей -CO-NH- по схеме:
Нитрилы R-С-=N – органические соединения, в которых углеводородный радикал связан с группой –C-=N (циан),формально являющиеся C-замещенными производными синильной кислоты HC≡N. Нитрилы обычно рассматриваются как производные соответствующих кислот(CH 3 -CN – нитрил уксусной кислоты (ацетонитрил)). Номенклатура: как производные соответствующих карбоновых кислот, например, CH3C≡N — ацетонитрил (нитрил уксусной кислоты), C6H5CN — бензонитрил (нитрил бензойной кислоты). В систематической номенклатуре для именования нитрилов используется суффикс карбонитрил, например, пиррол-3-карбонитрил.
Основным способом получения нитрилов является дегидратация амидов на кислотных катализаторах в присутствии водоотнимающих реагентов:
Гидролизом нитрилов получают карбоновые кислоты:
При восстановлении нитрилов образуются первичные амины:
Дата публикования: 2015-03-29; Прочитано: 2068 | Нарушение авторского права страницы
studopedia.org — Студопедия.Орг — 2014-2018 год.(0.001 с)…